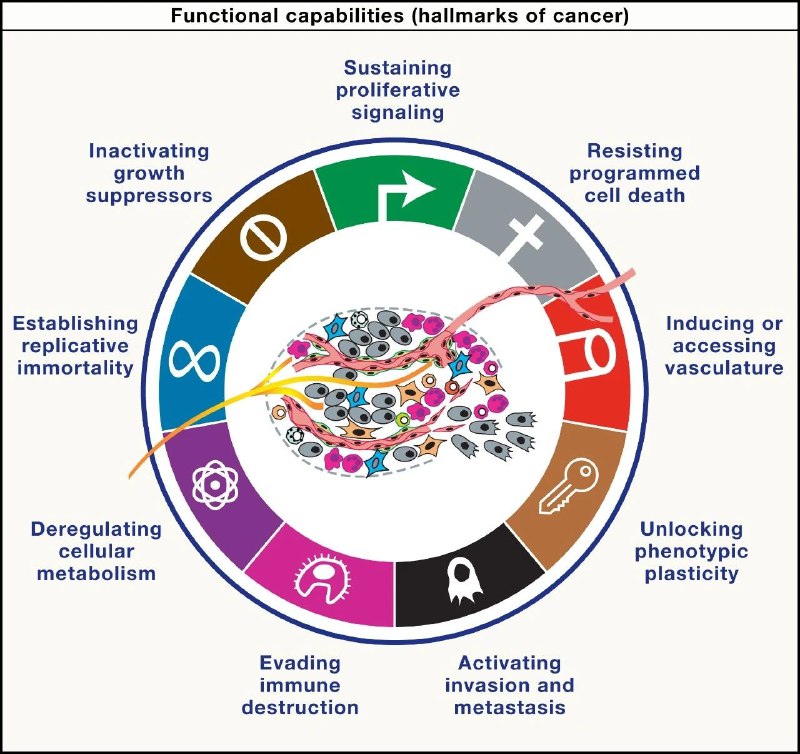
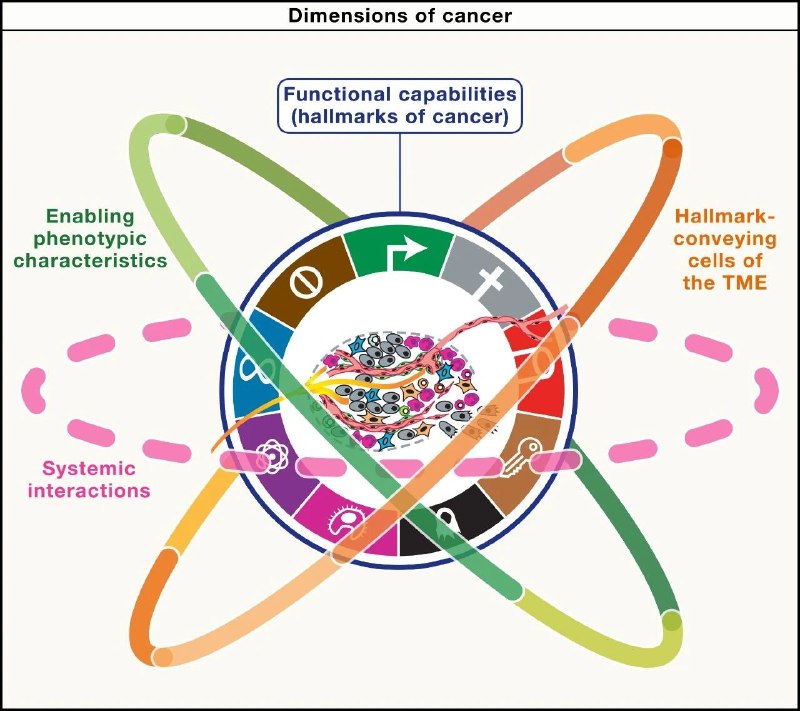
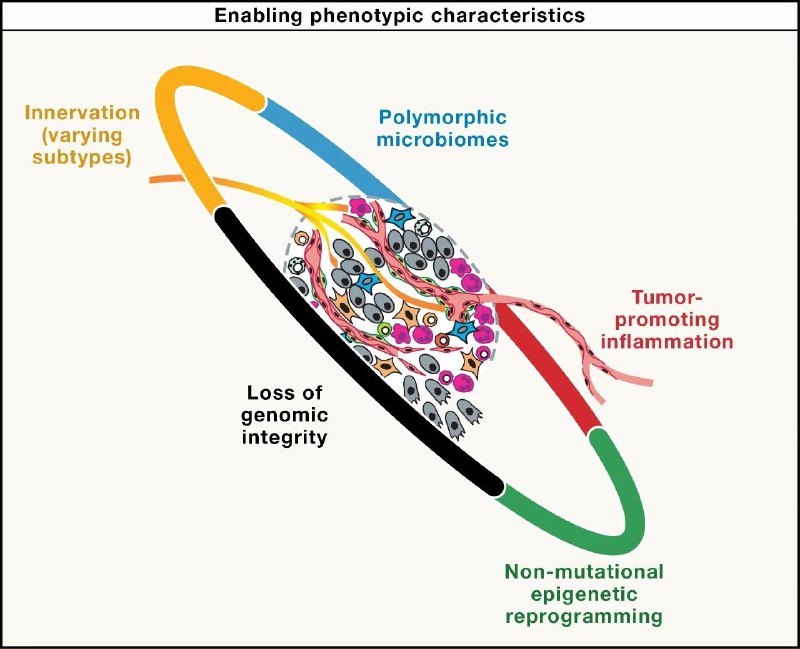
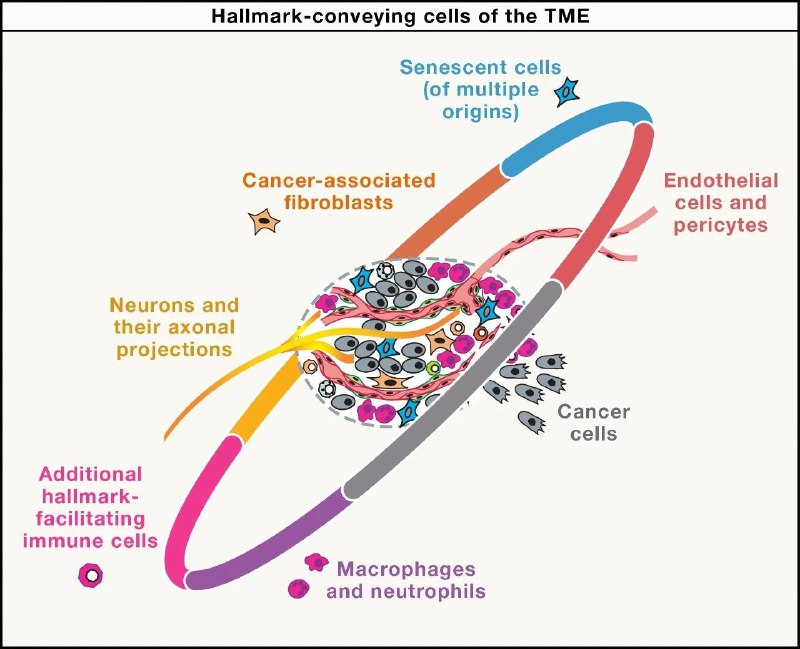
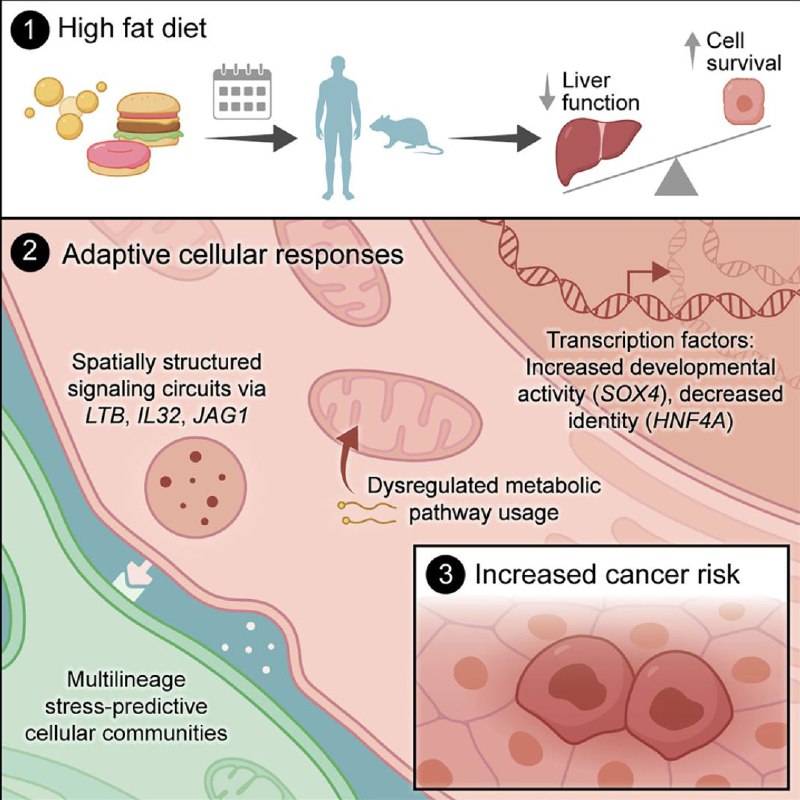
肝脏的无奈妥协:高脂饮食等慢性代谢压力竟为肿瘤发生埋下伏笔肝脏是我们体内的代谢工厂,负责解毒和合成。但在高脂饮食带来的长期的营养失衡或代谢压力下,肝细胞会死亡引发脂肪性肝炎(MASH),而那些幸存下来的细胞会发生什么变化?最新的一项研究揭示了它们为了生存所付出的代价。
研究人员利用跨物种纵向单细胞多组学技术发现,持续的高脂饮食带来的代谢压力迫使非癌变的肝细胞降低成熟功能,转而激活发育和癌症相关的程序。这种适应过程由特定的主调控因子驱动,它们在压力下促进细胞增殖,虽然短期内帮助细胞存活,却直接为未来的肿瘤发生“铺平了道路”。
此外,通过对人类组织的空间转录组学分析,研究还揭示了塑造这种压力反应的多细胞群落结构。这项发现阐明了细胞应对慢性压力的早期适应机制如何演变为癌症风险,为未来针对代谢性肝病的干预提供了新的核心靶点。
肝脏:为了活命只能被迫“黑化”🤯
来源:
Cell#肝脏 #代谢压力 #肿瘤发生 #Cell🧬 频道 |
🧑🔬 群组 |
📨 投稿