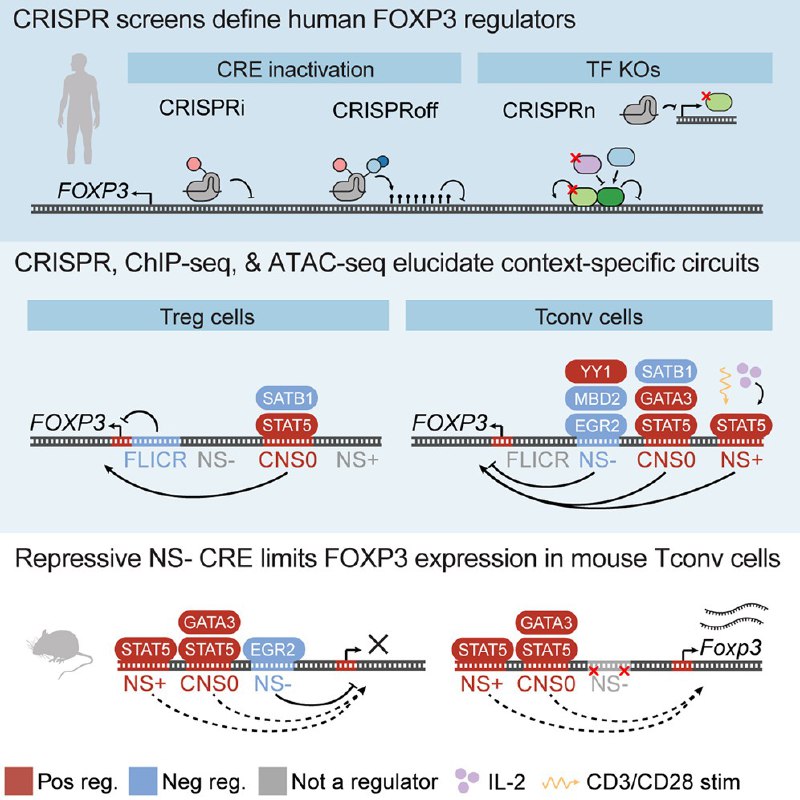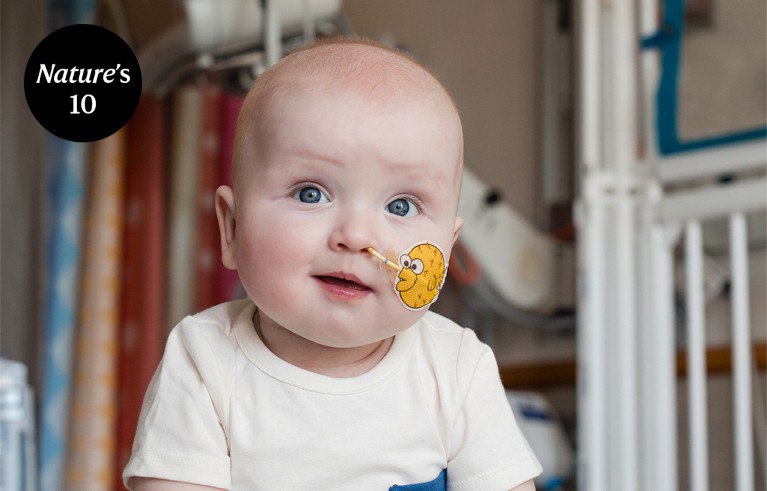
基因编辑技术再次创造医学奇迹,一名患有罕见遗传病的婴儿通过世界首例个性化CRISPR疗法获得新生。KJ Muldoon在2024年8月出生后不久被诊断出患有氨甲酰磷酸合成酶1缺乏症(CPS1 deficiency),这是一种极其罕见的基因缺陷,会导致体内有毒氨积聚,损害大脑,约50%的患者会在婴儿期夭折。
研究团队使用CRISPR基因编辑的一种变体——碱基编辑技术,精准定位并修复了患者基因组中那一个导致疾病的错误碱基。这种超个性化疗法从设计到完成仅用了6个月,远低于原计划的18个月。2025年2月25日,KJ接受了首次治疗,现在他的蛋白质耐受性已提高,但仍需药物和定期监测以控制氨水平。
这项突破标志着基因治疗从"通用型"向"超个性化"的重大转变,但也面临制造复杂、成本高昂的挑战。虽然这种疗法目前只能针对特定患者,但它为治疗其他罕见遗传病开辟了新途径,展示了基因编辑技术在精准医疗领域的巨大潜力。
基因编辑界的"量体裁衣"服务,拯救一个生命只需修改30亿个碱基中的一个!
来源:Nature
#基因编辑 #CRISPR #个性化医疗 #罕见病 #精准医疗
🧬 频道 | 🧑🔬 群组 | 📨 投稿
👍 13 ❤️ 3 🥰 3