科学家揭示毛囊生长的“拉力”机制:毛发生长原来是细胞被“拽”出来的
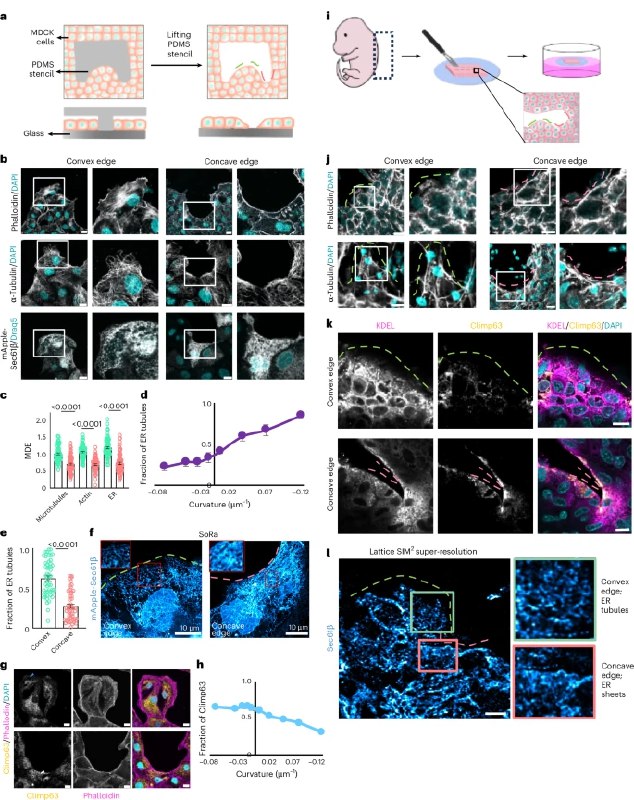
我们常以为头发长长是因为细胞不断分裂,但一项新研究颠覆了这一认知。科学家通过3D活体成像技术,观察体外培养的人类毛囊,发现外根鞘细胞会以螺旋状向下移动进入毛囊底部,而毛囊底部的细胞则向上流动,最终形成毛发。这表明毛发生长可能涉及一种“拉力”机制。
研究团队进一步发现,毛囊外层细胞的移动速度与细胞分裂率直接相关——移动越快的地方,细胞分裂越活跃。通过流体动力学模拟和实验干预,他们提出模型:外根鞘细胞的向下运动产生拉力,将毛囊底部的细胞向上“拽”,从而推动毛发向外生长。这种机制与动物毛囊中干细胞分化的模式一致,但首次在人类中验证。
这一发现为理解毛发生长提供了新视角,可能有助于开发更有效的脱发治疗或毛囊再生技术。不过,研究是在体外培养的毛囊中进行,体内环境更为复杂,未来需要更多体内实验来验证这一模型。目前结果仍需更多样本和长期研究支持。
来源:Nature communications
#毛囊生长 #细胞动力学 #生物力学 #毛发生长机制 #科学发现
via: 热心群友
🧬 频道 | 🧑🔬 群组 | 📨 投稿
我们常以为头发长长是因为细胞不断分裂,但一项新研究颠覆了这一认知。科学家通过3D活体成像技术,观察体外培养的人类毛囊,发现外根鞘细胞会以螺旋状向下移动进入毛囊底部,而毛囊底部的细胞则向上流动,最终形成毛发。这表明毛发生长可能涉及一种“拉力”机制。
研究团队进一步发现,毛囊外层细胞的移动速度与细胞分裂率直接相关——移动越快的地方,细胞分裂越活跃。通过流体动力学模拟和实验干预,他们提出模型:外根鞘细胞的向下运动产生拉力,将毛囊底部的细胞向上“拽”,从而推动毛发向外生长。这种机制与动物毛囊中干细胞分化的模式一致,但首次在人类中验证。
这一发现为理解毛发生长提供了新视角,可能有助于开发更有效的脱发治疗或毛囊再生技术。不过,研究是在体外培养的毛囊中进行,体内环境更为复杂,未来需要更多体内实验来验证这一模型。目前结果仍需更多样本和长期研究支持。
头发原来是被“拽”出来的,这下剪头发后感觉头发更长得更快有科学解释了!
来源:Nature communications
#毛囊生长 #细胞动力学 #生物力学 #毛发生长机制 #科学发现
via: 热心群友
🧬 频道 | 🧑🔬 群组 | 📨 投稿
🤔 5