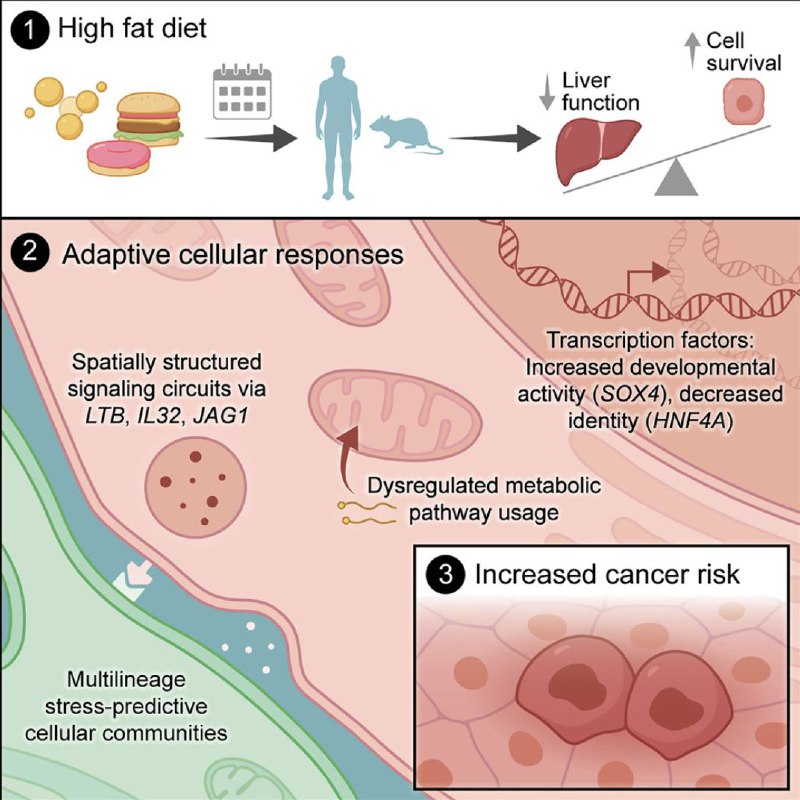
衰老的肝脏可能通过外泌体助长癌症转移
随着年龄增长,癌症成为65岁以上人群的主要死因,而肿瘤转移是关键元凶。过去认为,衰老相关的代谢变化会增加转移风险,但具体机制一直不明。最新研究揭示,衰老的肝细胞可能通过释放一种“隐形信使”——外泌体,来助长癌症转移。
研究团队在老鼠实验中发现,衰老肝脏中P2X7受体表达升高,导致外泌体产生增加。这些外泌体携带miR-25、miR-92a等分子,通过血液循环到达原发肿瘤,上调肿瘤细胞内的PTEN和LATS2等基因表达,促进上皮间质转化(EMT),从而增强肿瘤的侵袭和转移能力。临床样本也显示,老年患者转移性肿瘤中这些miRNA靶基因表达降低,EMT特征更明显。
该研究为理解衰老与癌症转移的关联提供了新视角,并指出靶向衰老细胞或外泌体相关miRNA可能成为干预策略。不过,目前研究主要基于小鼠模型,临床样本数量有限,未来需要更多人体试验来验证这些发现,并探索如何有效阻断这一过程。
来源:Nature aging
#衰老 #癌症转移 #外泌体 #miRNA #肝细胞
🧬 频道 | 🧑🔬 群组 | 📨 投稿
随着年龄增长,癌症成为65岁以上人群的主要死因,而肿瘤转移是关键元凶。过去认为,衰老相关的代谢变化会增加转移风险,但具体机制一直不明。最新研究揭示,衰老的肝细胞可能通过释放一种“隐形信使”——外泌体,来助长癌症转移。
研究团队在老鼠实验中发现,衰老肝脏中P2X7受体表达升高,导致外泌体产生增加。这些外泌体携带miR-25、miR-92a等分子,通过血液循环到达原发肿瘤,上调肿瘤细胞内的PTEN和LATS2等基因表达,促进上皮间质转化(EMT),从而增强肿瘤的侵袭和转移能力。临床样本也显示,老年患者转移性肿瘤中这些miRNA靶基因表达降低,EMT特征更明显。
该研究为理解衰老与癌症转移的关联提供了新视角,并指出靶向衰老细胞或外泌体相关miRNA可能成为干预策略。不过,目前研究主要基于小鼠模型,临床样本数量有限,未来需要更多人体试验来验证这些发现,并探索如何有效阻断这一过程。
衰老的肝脏也可能“帮倒忙”🤔
来源:Nature aging
#衰老 #癌症转移 #外泌体 #miRNA #肝细胞
🧬 频道 | 🧑🔬 群组 | 📨 投稿
😢 4 🤬 2 ❤️ 1