肝脏“重启”免疫?科学家发现衰老免疫的“救星”
随着年纪增长,我们常发现免疫力下降,容易生病、疫苗效果变差,传统方法改善有限。最近一项发表在《自然》的研究发现,肝脏可能成为“免疫救星”——通过暂时调整自身功能,帮助恢复衰老的免疫系统。
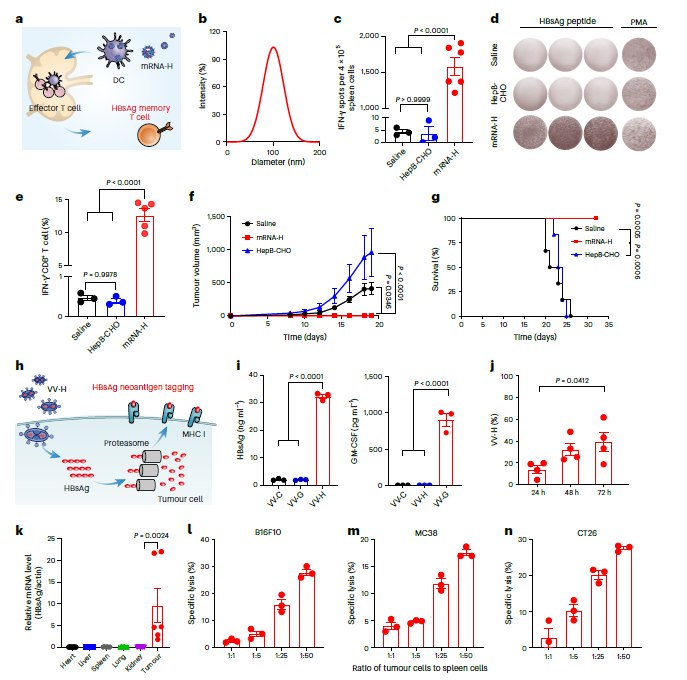
研究团队通过多组学分析年轻与衰老小鼠的免疫微环境,发现Notch、FLT3L和IL-7等关键通路随年龄下降。他们给衰老小鼠的肝细胞递送编码这些因子的mRNA,结果肝脏“生产”出更多免疫信号,扩增淋巴祖细胞,促进新T细胞在胸腺生成,补充外周T细胞库,同时增加树突状细胞数量和功能。实验显示,这种处理能提升疫苗反应和抗肿瘤免疫,效果可逆且不引发自身免疫问题。
这项研究为mRNA免疫调节提供了新思路,相比传统细胞因子疗法,mRNA策略更安全、可逆。不过目前仅在老鼠模型中验证,未来是否适用于人类、长期安全性等仍需更多研究,但为延缓衰老免疫衰退带来了希望。
来源:Nature
#衰老免疫 #肝脏 #mRNA疗法 #T细胞 #疫苗反应
🧬 频道 | 🧑🔬 群组 | 📨 投稿
随着年纪增长,我们常发现免疫力下降,容易生病、疫苗效果变差,传统方法改善有限。最近一项发表在《自然》的研究发现,肝脏可能成为“免疫救星”——通过暂时调整自身功能,帮助恢复衰老的免疫系统。
研究团队通过多组学分析年轻与衰老小鼠的免疫微环境,发现Notch、FLT3L和IL-7等关键通路随年龄下降。他们给衰老小鼠的肝细胞递送编码这些因子的mRNA,结果肝脏“生产”出更多免疫信号,扩增淋巴祖细胞,促进新T细胞在胸腺生成,补充外周T细胞库,同时增加树突状细胞数量和功能。实验显示,这种处理能提升疫苗反应和抗肿瘤免疫,效果可逆且不引发自身免疫问题。
这项研究为mRNA免疫调节提供了新思路,相比传统细胞因子疗法,mRNA策略更安全、可逆。不过目前仅在老鼠模型中验证,未来是否适用于人类、长期安全性等仍需更多研究,但为延缓衰老免疫衰退带来了希望。
肝脏也能当免疫“加油站”?🤯
来源:Nature
#衰老免疫 #肝脏 #mRNA疗法 #T细胞 #疫苗反应
🧬 频道 | 🧑🔬 群组 | 📨 投稿