
👍 5 ❤️ 1




脑癌的“小团伙”终于被拆穿啦!🧠
细菌也能当药厂?看来以后得小心肠道里的“小药丸”了🤣
核受体学了二十年说不可成药,结果人家就是"逆向操作"了一下,科研圈专治各种不服。😂
原来肿瘤疫苗的“刹车”是视黄酸信号,科学真有意思🧪
肿瘤细胞:这线粒体不错,🇰🇷了🤪
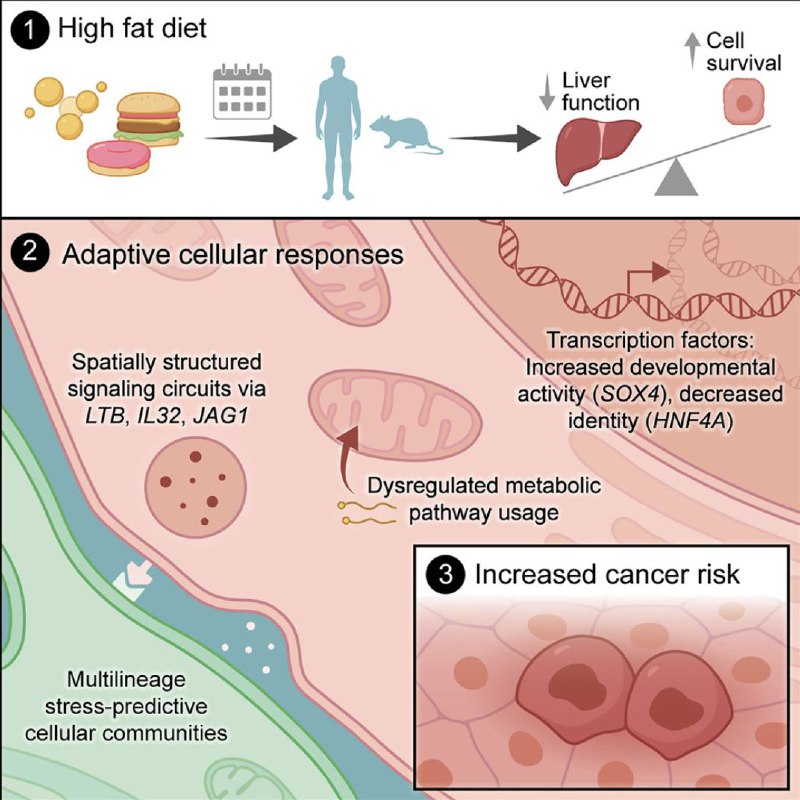
肝脏:为了活命只能被迫“黑化”🤯
传统化疗是“地毯式轰炸”,好坏细胞一起遭殃。精准医疗就像是配了 GPS 的巡航导弹,直捣癌细胞老巢。

免疫系统:太黑了,啥也看不见。😎
科学家:给你打个“照明弹”(mRNA 疫苗)!💥
免疫系统:嚯!亮堂了!原来肿瘤搁那儿藏着呢!🫵