
👍 5 ❤️ 1




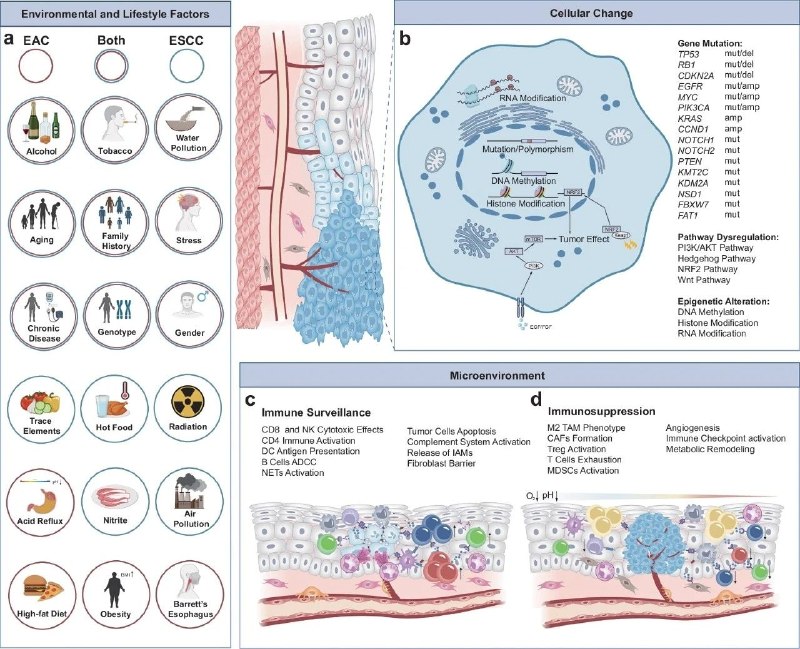
脑癌的“小团伙”终于被拆穿啦!🧠
药物也在细胞里“搞小团体”?🤔
细菌也能当药厂?看来以后得小心肠道里的“小药丸”了🤣
细菌变“免疫增强剂”?肿瘤治疗新思路,有点像给肿瘤“打气”呢!🧪
肿瘤科的隐藏 boss,很多时候不是癌细胞,是血栓 😄
核受体学了二十年说不可成药,结果人家就是"逆向操作"了一下,科研圈专治各种不服。😂
终于有能模拟人脑免疫反应的模型了,以后研究免疫治疗不用再猜了🧠

原来激素还能这么影响肿瘤免疫,看来得注意激素平衡啦🤔
原来肿瘤疫苗的“刹车”是视黄酸信号,科学真有意思🧪
肿瘤细胞:这线粒体不错,🇰🇷了🤪
肿瘤细胞也能“自产自销”免疫武器?看来癌症免疫治疗要玩出新花样了🤖
原来免疫治疗“打不过”的元凶是这些“老态龙钟”的B细胞🤔
原来PD-L1还会“自残”?肿瘤细胞逃免疫的“小聪明”被揪出啦🤫

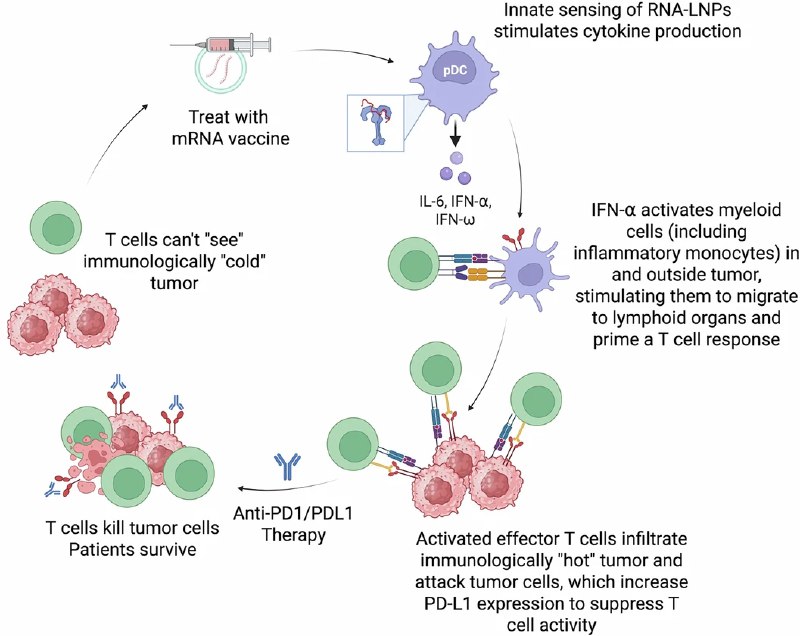
以前是对着肿瘤扔炸弹,现在是给免疫细胞发“通缉令”和“特种装备”,让它们自己去抓捕和消灭癌细胞。😈
传统化疗是“地毯式轰炸”,好坏细胞一起遭殃。精准医疗就像是配了 GPS 的巡航导弹,直捣癌细胞老巢。
原报告我放在评论区,接下来我也会分点解读这个报告😘感兴趣的也可以加组群讨论

免疫系统:太黑了,啥也看不见。😎
科学家:给你打个“照明弹”(mRNA 疫苗)!💥
免疫系统:嚯!亮堂了!原来肿瘤搁那儿藏着呢!🫵